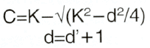Biometría y cálculo del poder dióptrico de las lentes intraoculares
La biometría es una técnica no invasiva, rápida e inocua que nos permite realizar mediciones tanto del globo ocular, en cualquier segmento del eje óptico, como de la órbita. Pero vamos a centrarnos básicamente en el interés que tiene la biometría para el cálculo del poder dióptrico de las lentes intraoculares.
El primer cirujano que implantó una lente intraocular fue Ridley (1), en 1949, pero esta práctica no fue ampliamente aceptada hasta los años setenta. El empleo de la lente intraocular supuso un importante beneficio para el paciente intervenido de catarata, dado que éstas son la opción más adecuada para la corrección óptica posquirúrgica al proporcionar una imagen retiniana de tamaño prácticamente fisiológico. Las lentes intraoculares, independientemente de su colocación, no superan nunca una magnificación del 4%. El uso de gafas o lentes de contacto correctoras en los pacientes afáquicos les produce una magnificación de las imágenes que puede llegar a ser del 25%-30% y del 12%, respectivamente. Debemos recordar que, cuando la diferencia de tamaño de las imágenes en la retina de cada ojo supera el 5%, aparece la aniseiconia.
Cálculo del poder dióptrico de las lentes intraoculares
El cálculo del poder dióptrico de las lentes intraoculares (LlO) es una parte esencial del examen preoperatorio en la cirugía de la catarata (2). Viene determinado por los factores que se exponen en el Cuadro 1. Se calcula mediante el empleo de fórmulas teóricas y fórmulas empíricas. Tanto las unas como las otras son perfectamente válidas para el cálculo del poder dióptrico de las lentes intraoculares, sin que se hayan encontrado diferencias estadísticas entre ambos métodos (3). Fórmulas teóricas. Este tipo de fórmulas derivan, en definitiva, de la geometría óptica y emplean constantes teóricas. Son todas ellas muy similares. En el Cuadro 2 se presentan las variables que emplean. Todas las fórmulas existentes se basan en el siguiente esquema y son válidas para ojos cuya longitud axial esté comprendida entre 22 y 22,45 mm:
P: Poder dióptrico de la lente para la emetropía
n: Índice de refracción de los medios
L: Longitud axial del globo ocular
K: Curvatura corneal
C: Profundidad de la cámara posterior postoperatoria
En las fórmulas teóricas se asume que el grosor de la lente es 0, es decir, se desprecia. Para el cálculo de la profundidad postoperatoria de la cámara anterior se emplea la siguiente fórmula (4):
C: Profundidad de la cámara anterior postoperatoria
K: Radio de curvatura corneal
d': Diámetro del iris visible o de la córnea óptica
La diferencia entre las distintas fórmulas teóricas estriba en los factores de corrección empleados en el cálculo de los distintos parámetros de la fórmula. En el Cuadro 3 recogemos las principales fórmulas teóricas y sus autores (3).
Posteriormente, ha aparecido una segunda generación de fórmulas teóricas que logran una mayor exactitud que las fórmulas originales. Las fórmulas más destacadas son las creadas por Binkhorst, Hoffer y Shammas. También destacaremos la fórmula de Holladay, que supone una mejora importante respecto de las anteriores fórmulas teóricas. Ésta es una fórmula no lineal que introduce un nuevo concepto, denominado "factor quirúrgico", similar al valor de la constante A de la fórmula empírica SRK que más adelante explicaremos. Es especialmente útil cuando el paciente ha sido sometido previamente a cirugía refractiva (5).
Fórmulas empíricas
También llamadas fórmulas de línea de regresión. Se basan en el análisis retrospectivo o de regresión de los resultados de la refracción postoperatoria obtenida tras múltiples intervenciones quirúrgicas con implante de lentes intraoculares. Es decir, parten de la experiencia aportada por los oftalmólogos cirujanos en la relación existente entre el valor preoperatorio de la longitud axial, el poder dióptrico de la córnea, el poder dióptrico de la lente y el error refractivo postoperatorio. Para ello se emplean estudios estadísticos de análisis de regresión.
En las fórmulas empleadas se supone una relación lineal de las variables
empleadas con el poder dióptrico de la lente:
P: Poder dióptrico de la lente.
ALX: Longitud axial del globo ocular en milímetros.
A, B y C: Constantes propias de las lentes.
K: Promedio del poder dióptrico de la córnea.
Aún se puede simplificar más esta fórmula haciendo que B y C sean estándar en las lentes de igual diseño. Fueron Sanders-Retzlaft-Kraff quienes simplificaron esta fórmula, haciendo universales B y C. Actualmente se la conoce como "fórmula SRK" (Cuadro 4). En ella, la constante A varía según el tipo de lente que empleemos. Su valor es mayor cuanto menor sea la distancia entre la lente y la retina. Por ejemplo, el valor de A para una lente de cámara anterior tipo Kelman Multiflex es 115,3 y en una lente de cámara posterior tipo Jaffe JF3LRU es 116,8.
Cuadro 3
La fórmula SRK es bastante más sencilla que cualquiera de las fórmulas teóricas, de ahí que su uso se haya extendido tanto. Presenta también la ventaja de obviar la profundidad de la cámara anterior. Es una fórmula con un valor predictivo bastante exacto para ojos con una ALX comprendida entre los 22 y los 22,5 mm. Sin embargo, no es tan exacta en ojos de tamaño más extremo, tendiendo a dejar hipocorregidos los ojos cortos e hipercorregidos los ojos largos. Para solventar este problema, se desarrolló una nueva fórmula, la SRK-ll. No es más que una simple modificación de su predecesora. En ella se suma o se resta a la constante A un valor que dependerá de la longitud del ojo. Se expresa en el Cuadro 5.